¿Por qué es tan criticada la hibridación in situ Kappa/lambda?
 2024-06-13
2024-06-13
Por admin

Métodos de detección de Kappa/Lambda
La detección de Kappa/Lambda se realiza habitualmente utilizando cuatro métodos en el laboratorio: hibridación in situ, inmunohistoquímica, citometría de flujo y PCR.
Hibridación in situ
El reactivo de sonda de cadena Kappa/Lambda es un reactivo especializado utilizado en el método de hibridación in situ. Con el fin de encontrar la secuencia de ARNm κ:λ de forma más precisa y sensible, se dirige específicamente a ese gen. Es muy útil que este reactivo pueda utilizarse con una gama más amplia de materiales. Esto lo hace útil para muchas tareas diferentes en patología molecular y diagnóstico clínico.
Citometría de flujo
La citometría de flujo es un proceso relativamente sencillo que consiste en preparar y etiquetar muestras de tejido antes de analizarlas con una máquina. Como parte de este método, se utilizan anticuerpos fluorescentes monoclonales para marcar determinadas proteínas en la superficie y el interior de las células. Con este método se pueden encontrar las proteínas diana de forma muy específica. Además, es menos probable que los sesgos individuales afecten a la interpretación de los resultados, lo que lo hace más sensible. Sin embargo, es importante tener en cuenta que para el análisis por citometría de flujo se necesitan muestras de tejido frescas que no hayan sido fijadas.
Inmunohistoquímica
Inmunohistoquímica (IHC) es una técnica bien establecida que requiere un equipo mínimo. Se utiliza habitualmente para marcar muestras fijadas en formol e incluidas en parafina (FFPE). Sin embargo, una limitación de la IHC es la posible interferencia de las inmunoglobulinas (Ig) del mesénquima debido a la naturaleza secretora de los anticuerpos. Esto podría modificar la especificidad de los datos de coloración. La IHC también puede dificultar la búsqueda de inmunoglobulinas que no estén presentes en grandes cantidades. A pesar de estos problemas, la IHC sigue siendo un método útil para el estudio y el diagnóstico porque nos permite ver dónde y cómo se producen las proteínas en las muestras de tejido.
PCR
Al emplear el reacción en cadena de la polimerasa (PCR) es necesario enviar las muestras a un laboratorio molecular especializado para su análisis. Como parte de este proceso, se extraen ácidos nucleicos de las muestras. Es importante tener en cuenta que el estudio PCR no dice nada sobre tejidos o células. Su objetivo principal es encontrar y aumentar patrones específicos de ADN o ARN. Mucha gente en investigaciones y biología molecular utiliza la PCR para encontrar y aprender sobre material genético.
Cabe señalar que el recuento preciso debe ser el factor principal para la detección de Kappa/Lambda,
Ventajas de la hibridación in situ de Kappa/Lambda
En patología molecular, la hibridación in situ es una buena forma de obtener datos de marcaje claros y precisos. En comparación con inmunohistoquímicaEste método es mejor porque permite ver las partes de las células con mayor claridad y exactitud. La claridad de tinción conseguida mediante la hibridación in situ permite un análisis más exhaustivo de la muestra, lo que conduce a un diagnóstico más preciso. Este método es aplicable a una amplia gama de tipos de muestras, lo que lo convierte en una herramienta versátil en diversos procedimientos de diagnóstico.
Además, la hibridación in situ es más sensible y específica que otros métodos como la citometría de flujo y la inmunohistoquímica. Esta alta sensibilidad y especificidad significan que la hibridación in situ puede detectar incluso cambios diminutos en la estructura celular, lo que la convierte en una herramienta muy eficaz para diagnosticar enfermedades en sus fases más tempranas. Especialmente importante para diagnosticar enfermedades como el cáncer relacionado con células plasmáticas y el mieloma múltiple, en las que su detección precoz puede suponer una gran diferencia en la evolución del paciente. Además de sus resultados de tinción superiores y su alta sensibilidad y especificidad, la hibridación in situ también facilita el recuento y la determinación de si se ha producido una proliferación restringida de cadenas ligeras. Esta característica es muy importante para diagnosticar correctamente muchas enfermedades diferentes. Podemos hacernos una mejor idea de cómo se está propagando la enfermedad con la hibridación in situ porque ofrece una imagen clara y completa de la estructura de las células. Al final, esto ayuda a elaborar mejores planes de tratamiento. Así pues, la hibridación in situ tiene ventajas que van más allá de su capacidad de diagnóstico. También ayuda mucho a mantener las enfermedades bajo control y a tratarlas.
Kit de sondas Kappa/Lambda (ISH) de Celnovte

La empresa Celnovte Celnovte, fundada en 2010, es una empresa de alta tecnología centrada en el estudio, la creación, la producción y la distribución de herramientas y materiales precisos para la detección de tumores, con especial atención a la detección precoz, el diagnóstico preciso, la asociación de fármacos y el seguimiento de los tumores durante el tratamiento. Celnovte ha establecido una completa cadena industrial que integra I+D, producción, ventas y servicios, con el objetivo de convertirse en un proveedor líder de soluciones integrales para productos de diagnóstico de patología tumoral tanto a nivel nacional como internacional. Por ejemplo, CNT360 Tinción IHC&ISH totalmente automática, CNT 620 Goteadora y Cubridora HE Totalmente Automáticay otros instrumentos de diagnóstico de alta calidad son muy populares. La empresa ha obtenido las certificaciones ISO9001, ISO13485 y CE-ID de la UE, lo que demuestra su compromiso con la calidad y la innovación.
Celnovte lanza un Kit de sondas Kappa/Lambda (ISH). Cuando se utiliza la metodología de hibridación in situ, puede generar una tinción clara y un rendimiento superior en comparación con la inmunohistoquímica con el avance de la tecnología de anticuerpos secundarios microagregados MicroStackerTM. Evita las interferencias en el recuento de fondo causadas por la tinción inespecífica de inmunoglobulinas en la sustancia intercelular inmunohistoquímica.
Muestra de linfoma:
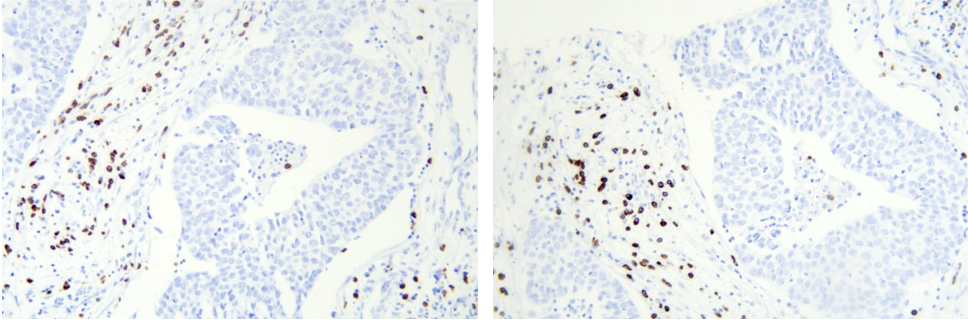
Kit de sonda Kappa y kit de sonda Lambda
Escenario de aplicación
κ y λ son dos tipos de cadenas ligeras en inmunoglobulinas. La proporción de células plasmáticas que expresan diferentes cadenas ligeras κ:λ en los ganglios linfáticos normales es de aproximadamente 2:1. La expresión restringida de kappa o lambda sugiere proliferación monoclonal y formación de tumores. El proyecto de detección de hibridación in situ Kappa/Lambda puede detectar la proporción κ/λ en células plasmáticas para confirmar si se produce proliferación clonal κ o λ (es decir, expresión restringida de esa cadena ligera) en el tejido linfoide.
El proyecto de detección de hibridación in situ Kappa/Lambda se utiliza ampliamente en el diagnóstico del mieloma múltiple. También se utiliza en el diagnóstico de enfermedades relacionadas con las células plasmáticas, como el linfoma extranodal con diferenciación de células plasmáticas, la gammapatía monoclonal de significado indeterminado (MGUS), la amiloidosis AL, la macroglobulinemia de Waldenstrom, el linfoma difuso de células B grandes (DLBCL), el linfoma de células del manto (MCL), leucemia linfocítica crónica (LLC)/linfoma linfocítico pequeño (LLCP), linfoma de la zona marginal (LZM), linfoma de Burkitt (BL) y otros subtipos comunes de linfoma no Hodgkin, linfoma de Hodgkin, linfoma del centro folicular, leucemia de células B precursoras o leucemia linfoblástica aguda.
Principio de la Kit de sondas Kappa/Lambda (ISH)
El proceso de sondeo en el proyecto de detección de hibridación in situ Kappa/Lambda se basa en el reconocimiento específico de hibridación de la sonda marcada con digoxigenina (DIG) derivados de plantas. Mediante el uso de una cascada de señales que incluye anticuerpos secundarios, este enfoque innovador permite la detección sensible y precisa de células kappa/lambda. Este método puede detectar de forma fiable y precisa el mieloma múltiple y otras enfermedades relacionadas con las células plasmáticas centrándose en las secuencias de ARNm kappa/lambda. Una herramienta de patología molecular accesible y práctica, el sistema cromogénico HRP-DAB permite la observación de los datos de tinción bajo un microscopio óptico. Con su práctico valor clínico y patológico, esta tecnología, incluida la ampliamente adoptada hibridación in situ EBER, se ha convertido en el patrón oro para el diagnóstico de la infección por VEB en patología tisular. En definitiva, el proyecto de detección por hibridación in situ Kappa/Lambda proporciona resultados muy específicos y sensibles, que ayudan en la identificación y el estudio de linfomas y enfermedades asociadas.
Características del kit de sondas Kappa/Lambda (ISH)
Alta sensibilidad: Se dirige a secuencias de ARNm kappa/lambda y utiliza un innovador sistema cromogénico de anticuerpos secundarios poliméricos.
Alta especificidad: Utiliza marcaje DIG derivado de plantas y secuencias de sonda optimizadas.
Buena estabilidad: Sigue los procesos de producción SOP y presenta una buena estabilidad térmica.
Fácil de utilizar: Proporciona protocolos de validación estables, con sólo dos pasos adicionales en comparación con la inmunohistoquímica, lo que hace que sea cómodo de usar.
Fácil de interpretar: Proporciona imágenes de control positivo para una localización precisa de la tinción.
Mayor flexibilidad: Disponibles como kits de reactivos manuales y automatizados, compatibles con tinción dual.
Procedimiento experimental
Digestión enzimática - Hibridación de sondas - Incubación de anticuerpos primarios - Incubación de anticuerpos secundarios - Tinción cromogénica DAB
En este procedimiento, sólo se añaden los pasos de digestión enzimática e hibridación de la sonda en comparación con la inmunohistoquímica, ¡lo que resulta más cómodo de llevar a cabo!









